Malyugina 4
Grupuri și subgrupuri
Malyugina 4. Structura sistemului periodic. Grupuri și subgrupuri.
Sistemul Periodic este format din șapte perioade de zece rânduri și opt grupe, fiecare dintre acestea fiind împărțit în subgrupuri primare și secundare.
Grupul a sistemului periodic al elementelor chimice (PSKHE) - serie verticală a elementelor chimice aranjate în nucleul atomic ascendent încărcare, care sunt aceleași în cele mai înalte compușii lor valența egal cu numărul de grup. Numărul grupului este indicat printr-un numeral roman.
Fig.1. Grupuri PSKHE

De exemplu. atom de sodiu (Z = 11) are cea mai mare valenței I, t I este situat într-o grupă PSKHE și un atom de clor (Z = 17) -... VII, m este un grup în VII.
De exemplu. toate elementele din grupa II au cea mai mare valența II, astfel încât formula de oxizi ai elementelor superioare ale perioadei II în general RO (MgO, CaO, BaO, ZnO și m. p.). Toate elementele perioadei IV exponat cea mai mare valență egal IV, astfel formula de oxizi ai elementelor superioare ale perioadei IV în general RO2 (CO2, SiO2, TiO2, GeO2 și m. P.).
O excepție este de a lăsa elementele specificate în tabelul 1.
În exemplul de realizare, perioade scurte grupe de sistem periodice sunt împărțite în subgrupe - principale (sau subgrupa A) și lateral (subgrupul B).
Root subgrupă începe cu elementele prima și a doua perioade, partea - cu elemente ale perioadei IV.
Acasă subgrup conține elemente ale ambelor perioade mici și mari. subgrup incidental conține elemente numai pe perioade mari.
Fig. 2. Principalele și subgrupurile din grupa 1
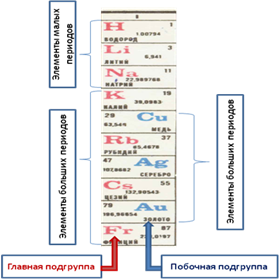
Fig. 3. Unele subgrupuri majore PSKHE
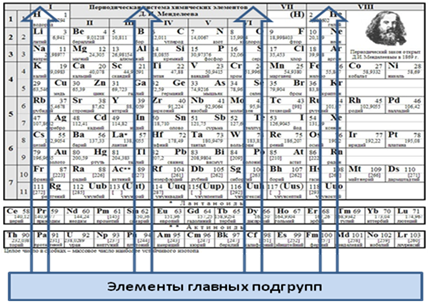
Fig. 4. Unele PSKHE subgrup din partea
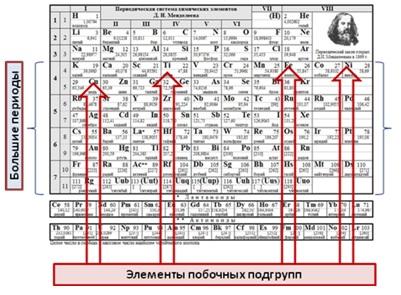
În sistemul periodic - 8 și 10 ale principalelor subgrupurile (I - VII grupuri sunt împărțite în două grupe principale - și secundare). grupa VIII este alcătuită din unul principal (gaze inerte) și trei laterale (subgrupul de fier, subgrupa podrguppa cobalt și nichel).
Subgrupul au, de asemenea, numele elementului cu cel mai mic număr de secvență (de obicei, pe un element de a doua perioade de principal și sub-element al perioadei a patra a subgrupurilor).
Elementele un subgrup au proprietăți chimice similare. t. k. subgrupe de elemente similare una cu alta în structura nivelului electronic extern.
Schimbări regulate observate în principalele subgrupe.
La fiecare subgrup principal în jos este metalic amplificată și proprietăți de atenuare a metaloid, de asemenea, de recuperare îmbunătățită și slăbesc proprietățile oxidante ale elementelor și compușilor formați de aceștia.
Toate elementele podochnyh subgrupuri sunt metale.
Testați-vă cunoștințele
1. Care sunt elementele structurale este sistemul periodic al elementelor chimice.
2. Ce este un artist?
3. Câte grupuri din tabelul periodic al elementelor chimice?
4. Elementele care perioadele sunt incluse în grupul principal?
5. Cât de multe subgrupuri în tabelul periodic?
6. Elementele care perioadele sunt incluse în subgrupele?
7. Pe cât de multe sub-divizat fiecare grup?
8. Ce face elementele unui grup?
9. Ce elemente ale unui subgrup?
10. Cum se schimbă proprietățile elementelor principale de grup de sus în jos?
11. Ce proprietati au elementele subgrupurilor?
12. Care grup conține un primar și trei subgrupuri secundare?
1. Din perioade rânduri, grupe și subgrupe.
2. Grupul - o serie verticală de elemente chimice aranjate în creșterea sarcina nucleelor atomice care au aceeași în cea mai mare valența conexiunile lor fiind egal cu numărul de grup.
4. mici și mari. Acasă subgrup perioadă mică începe elementul (I sau II). A se vedea. Figura 3.
6. Numai mari. Acasă subgrup începe cu perioada elementul IV. A se vedea. Figura 4.
7. I - VII grup sunt împărțite în două grupe - principal și lateral. grupa VIII constă dintr-unul principal - gaze inerte și trei laterale: subgrupă fier de cobalt subgrupă podrguppa și nichel.
8. În general, cu cât valența elementelor. Este egal cu numărul de grup, care este un element.
9. Proprietățile chimice, adică. K. Subgrupele de elemente similare una cu alta în structura nivelului electronic extern.
10. La fiecare subgrup principal în jos este din metal amplificat și proprietăți de atenuare a metaloid, de asemenea, de recuperare îmbunătățită și slăbesc proprietățile oxidante ale elementelor și compușilor formați de aceștia.
Sarcini pentru decizia independentă.
1. Într-un grup și sunt elemente podruppe cu numere atomice 6, 40, 26, 53, 80? Se specifică caracterul lor, numele rus, masa atomică relativă.
2. Scrieți simbolul, numele, numărul de ordine al elementului și masa atomică relativă a elementului, care este: a) în perioada III, subgrupa principal al Grupului VI; b) în perioada V din grupa de tranziție grupa II; c) VI este prezentat, subgrupul principal al grupului IV;
g) în perioada IV, grupa de tranziție grupa VII.
3. Scrieți simbolurile, numele și numerele de serie ale tuturor elementelor perioadelor mici, care sunt subgrupa principal din grupa IV.
4. Scrieți simbolurile, numele și numerele de serie ale tuturor elementelor care se află în sub-grupuri de grupa II.
5. Care sunt elementele principale subgrupa de elemente din grupa V sunt perioade lungi de timp? Scrie simbolurile lor, numele românești și numere de serie.
6. Ce element de: calciu sau bariu este proprietăți metalice mai accentuate și de ce?
7. Ce element de: sulf sau oxigen este proprietăți metalice mai pronunțată și de ce?
8. Care element din grupa VII al grupului principal este cel mai activ non-metal? De ce?
9. Care element din grupa principală Grupa I este metalul cel mai activ? De ce?
10. grupuri care ale sistemului periodic al elementelor sunt toate metalele?
11. Care grup este doar un non-metal?
12. Care din grupurile sistemului periodic al elementelor sunt toate nemetale?
13. forme de scriere, 25, 48, 13, în care aceste elemente au cel mai mare valența.
14. Scrieți oxizi formula elementelor din grupa principală grupa IV, în care acestea au cea mai mare valența.
3. Perioadele mici I - III. Subgrupa principal al elementelor IV grup includ perioade de carbon scurte C (Z = 6) și siliciu Si (Z = 14).
4. Incidentale subgrupul II grupa: Zn zinc (Z = 30), Cd cadmiu (Z = 48) este mercur Hg (Z = 80) A se vedea Fig.4.
5. perioade mari IV - VII. Subgrupa principal al elementelor grupului V sunt perioade mari sunt arsenic As (Z = 33), antimoniu Sb (Z = 51), bismut Bi (Z = 83).
6. Bariu. Bucurându-se de PSKHE. Ele sunt în același grup principal și subgrupa în partea de sus în jos principal există o întărire a proprietăților metalice. Bariu este mai mic decât calciu.
7. oxigen. Bucurându-se de PSKHE. Ele sunt în același grup principal și subgrupa în partea de sus în jos principal există o slăbire a proprietăților nemetalice. Oxigenul este mai mare decât sulf.
8. Fluor. Bucurându-se de PSKHE. Principalul Subgrupul de sus în jos există o slăbire a proprietăților nemetalice. Cel mai activ non-metal este la începutul grupului.
9. Franța. Principalul Subgrupul de sus în jos nu este îmbunătățită proprietăți metalice. Metalul cel mai activ este, la sfârșitul fiecărui grup.
10. I (cu excepția hidrogenului. Poziția T. K. său este ambiguă) și II.
12. Un astfel de grup nu este prezent, deoarece toate grupele laterale conțin elemente de subgrupă și toate subgrupurile - metale.